- E-mail : info_marketing@jindunchemical.cn
- Phone : +86 21 64057580
- Address : Shanghai China
Улучшенный процесс синтеза сукцината троглитазона, лекарства от диабета: минимизация образования примесей
Троглитазон сукцинат, новый пероральный ДПП-4 ингибитор, разработанный Takeda
Pharmaceuticals была одобрена для лечения диабета II типа в
Япония в марте26,2015.
Данные активности показали, что троглитазон сукцинат ингибирует ДПП-4 более
эффективнее, чем алоглиптин, другой препарат для лечения диабета II типа, разработанный Takeda.
Pharmaceuticals и ситаглиптин (торговое название: Genovel), тяжеловес
гипогликемический препарат, принадлежащий компании Merck Sharp & Dohme, и, кроме того,
селективность препарата была отличной.
Это связано с уникальным терапевтическим эффектом и хорошими рыночными перспективами троглитазона. сукцинат, что фармацевтические исследователи улучшают его
процесс подготовки и разработка новых процессов подготовки.
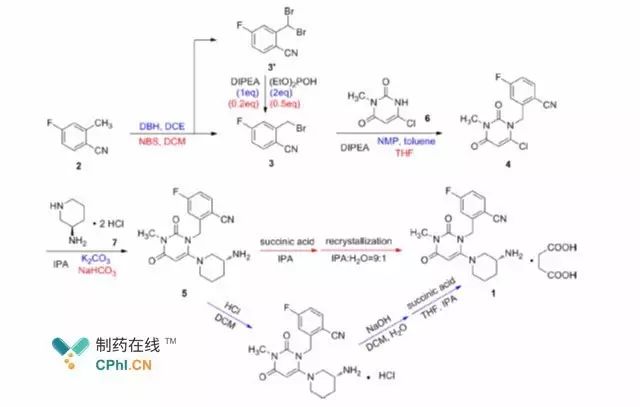
Фигура1 Процесс синтеза сукцината троглитазона
Такеда Фармасьютикал'Процесс синтеза троглитазона сукцината
показано на рисунке1. Маршрут основан на4-фтор-2-метилбензонитрил как
исходный материал и соединение3 получается после бромирования; сложный3 Можно
конденсироваться с промежуточным6 для получения соединения4, и далее сжато
с соединением7 для получения троглитазона, который может быть успешно получен
дальнейшее подкисление и перекристаллизация троглитазона сукцината.
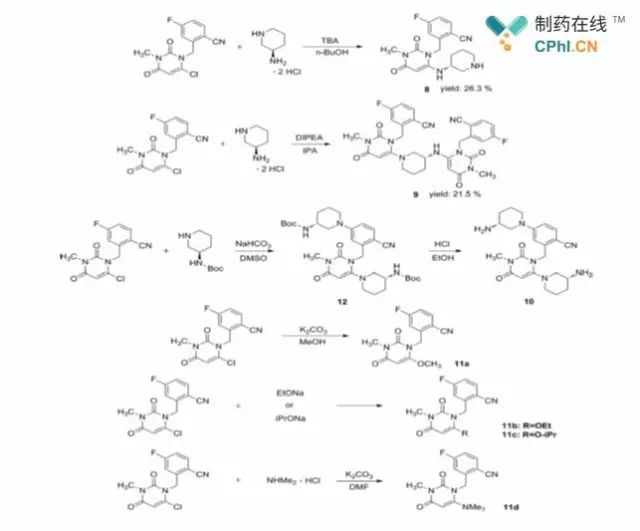
Фигура2 Синтез соединений8-11
Исследователи отметили, что стадия нуклеофильного замещения является ключевой для получения
высокая региоселективность реакции. Для конденсации соединения4 с
сложный7, чтобы избежать образования регионального изомера8 (Фигура2),
некоторые исследователи сообщали в2016 исследование улучшения оптимизации этого
шаг с использованием N-защищенного соединения7 сгущенный с соединением4, но это было
трудно избежать образования побочных продуктов, таких как продукты цианогидролиза
во время снятия защиты. В новом исследовании исследователи оптимизировали условия
из нескольких шагов, включая этот шаг.
В предыдущих отчетах исходное сырье2был отреагирован с1
эквивалент1,3-дибромо-5,5-диметилэтаноилмочевины в растворителе DCE с получением в основном
товар3&39;, который затем удаляли от одной молекулы HBr в присутствии диэтилового спирта.
фосфит, условия DIPEA для получения соединения3. В усовершенствованном процессе
исследователи успешно заменили класс токсичных растворителей, DCE, безвредным
растворителя, дихлорметана и путем корректировки эквивалентов и т. д. для достижения однореакторного
приготовление соединения3. Впоследствии исследователи изучили
нуклеофильное замещение более систематически, а образующиеся при этом примеси
шаг в основном составной8, сложный9 и соединение10 показано на рисунке2; когда
для этой реакции используется протонный растворитель (MeOH, EtOH, i-PrOH или DMF),
примеси11а-11д формируются. чтобы лучше изучить эти примеси, исследователи
также синтезировали их специально (рис.2).
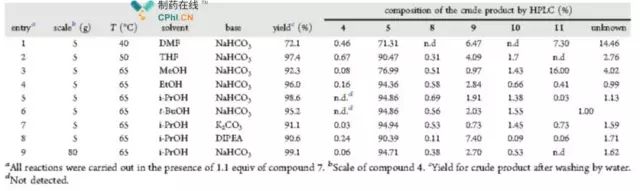
Фигура3 Скрининг условий нуклеофильного замещения
Как показано на рисунке3исследователи систематически проверяли стадия нуклеофильного замещения для таких условий, как температура реакции, использование растворителей и оснований, а также систематический анализ примесей с помощью ВЭЖХ. означает. Было обнаружено, что при использовании бикарбоната натрия в качестве основного катализатора изопропанол в качестве растворителя, а температура реакции65°С, реакция примеси могут быть сведены к минимуму с выходом99.1% (вход9).
Чистота сырого продукта троглитазона, синтезированного с использованием улучшенный процесс был до94%, что было большим улучшением по сравнению с исходным процесс. После дальнейшего подкисления и перекристаллизации получают триглиптина сукцинат. с чистотой99.93% был успешно получен.
В заключение, новый процесс успешно разработал эффективный и точный путь синтеза троглитазона сукцината от диабета, сокращение многих примесей в исходном процессе до очень низких пределов и успешно избежать использования токсичных растворителей, таких как1,2-дихлорэтан. Этот несомненно, принесет большую пользу для удовлетворения растущего рынка троглитазона сукцинат.
-
date
2022-10-10
-
location
Shanghai, China













































